《食品检验技术》课程实验教学大纲
一、课程概况(CourseOverview)
课程名称:食品检验技术
Course: Technology of Food Analysis
课程编号: 0081800032 适用学生: 生物科学、生物技术
Course Number:0081800032 Designed for: Bioscience, Biotechnology
学分:1 学时: 18 独立设课:否 理论课详见理论分册
Credit: 1 Class hour: 18 Independent course:no more information see speculative knowledge
预修课程:《生物化学》、《生物化学实验》、《分析化学》、《有机化学》
Preparatory Courses: Biochemistry、Biochemistry experiment, analytical chemistry, organic chemistry
二、课程简介(Course Descriptions)
食品检验技术实验内容包括食品检验样品的采集、制备、处理及食品中一些营养成分或有毒有害物质的定性、定量检验技术。
The part of lab isdesigned to acquaint the student with the practical operation on the measurement of some special components and residual drugs in food products.
三、实验项目一览表(Experiment project schedule)
序号 No. | 实验名称 Name | 每组人数 Members of each group | 实验 时数 Hours | 实验类型 验证∕综合∕设计 Course Type Verifying/Synthetic/Designing | 必做∕选做 Required Course /Elective Course |
1 | 食品中水分及灰分的测定 Determination of food water and ash content | 3 | 4 | 验证 Verifying | 必做 Required Course |
2 | 食品中蛋白质的测定 Determination of food protein content | 3 | 6 | 验证 Verifying | 必做 Required Course |
3 | 食品脂肪的测定 Determination of food lipid content | 3 | 4 | 验证 Verifying | 必做 Required Course |
4 | 食品中Vc的测定 Determination of food Vc content | 3 | 4 | 验证 Verifying | 必做 Required Course |
四、推荐教材及参考书目 (Recommended Teaching Materials and Reference Books)
1.推荐教材
《食品检测技术》,朱克永编,科学出版社,2007
Recommended Teaching Materials:
2.参考书目
《食品分析技术》,张意静主编,中国轻工业出版社,2006
《食品检验与分析》,黄伟坤等编著,轻工业出版社,1989
4、中华人民共和国国家标准,食品卫生检验标准理化部分,中国标准出版社,1986.
Reference Books:
五、考核与评价方式(Course Evaluation)
考核与评价方式:考查,详见理论课分册;考核方式根据实验操作情况与实验报告内容进行。
Course Evaluation: Evaluation
Course Evaluation: Evaluation
六、场地、设备与器材(Site, equipment and consumable materials)
场地:12-106
所用设备与器材:
电炉、灰化炉、精密天平、坩锅、坩锅钳、凯氏烧瓶、容量瓶、锥形瓶、酸式滴定管、消化炉、蒸馏仪、精密天平、自动搅拌器、移液枪、移液管、皮管、铁架台、铁夹、试管夹、索氏提取器、恒温水浴锅、干燥器、万能夹、干燥箱、电吹风、剪刀、滴定架、通风橱、蒸发皿、凯氏定氮仪、回流装置、碱式滴定管、研钵、棉线、脱脂棉、纱布、培养皿、烧杯、试剂瓶、旋转蒸发仪、恒流泵、橡皮塞、洗耳球等。
Equipment and consumable materials
electric cooker,calcination furnace, alytical balance, electric-heated thermostatic water bath, scissors, Kjeldahl flask, volumetric flask, conical beaker, acid burette, muffle, Glass distiller, stirring apparatus, refrigeratory, vacuum-drying oven, precision bala, nce, rotary evaporator, stink cupboard, etc.
撰写人:杨莉审定人:
《食品检验技术》课程实验项目1
食品中水分和灰分含量的测定
一、实验目的
学习和掌握食品中水分和灰分含量的测定方法和原理。
二、实验内容
食品中水分和灰分含量的测定。
三、实验原理
食品水分含量测定:食品中的水分受热以后,产生的蒸汽压高于空气在烘箱中的分压,使食品中的水分蒸发出来;由于不断的加热和排走水蒸汽,从而达到完全干燥的目的。根据样品在蒸发前后的失重在计算样品中的水分含量。
食品灰分含量测定:把一定量的样品经炭化后放入高温电炉内灼烧,使有机物质被氧化分解,以二氧化碳、氮的氧化物及水等形式逸出,而无机物质以硫酸盐、磷酸盐、碳酸盐、氯化物等无机盐和金属氧化物的形式残留下来,这些残留物即为灰分,称量残留物的重量即可计算出样品中总灰分的含量。
四、实验方法与步骤
1、佛手中水分含量的测定:
用清水洗净佛手,用干净纱布擦拭干净。
称取样品2 g,置于已干燥、冷却并称至恒重的坩锅中,移入95-105 ℃常压烘箱中,开盖烘干3小时后取出,加盖置干燥内冷却0.5小时后称重。再烘1小时左右,又冷却0.5小时后称重。重复此操作,直至前后两次质量差不超过2 mg即算恒重。测定结果按下式计算:
![]() 水分(%)=
水分(%)=
式中m1 ---------- 干燥前样品+称量瓶质量,g
m2 ---------- 干燥后样品+称量瓶质量,g
m3 ---------- 称量瓶质量,g
2、佛手中灰分含量的测定:
精确称取已充分干燥的佛手,精确至0.01g,置于已知恒重的瓷坩埚内,放在电炉上,瓷坩埚盖斜放,让佛手小心缓慢炭化,在炭化过程中应先在较低温度下灼烧至无烟,然后升高温度灼烧至试料呈灰白色,再放入灰化炉内,于600 ℃灼烧3 h,烘至白灰状即可。冷却后称重,计算灰分含量。。
五、实验要求
实验内容要求:(1)实验中高温操作较多,注意安全,防止烫伤事故发生;(2)水分测定中,佛手含有少量精油,在干燥过程中易挥发;但其含量较少,在本次实验中忽略不计;(3)灰分并不能准确表示食品中原来无机成分的总量,从这点出发通常把食品经高温灼烧后的残留物称之为粗灰分。
实验报告及考核评价要求:能正确、详尽书写实验目的、实验基本原理、操作步骤,正确客观的记录实验结果,并对实验结果(尤其是不理想的实验结果)进行分析和讨论。
六、场地、设备与器材
实验场地:待定
实验设备与器材:电炉、灰化炉、精密天平、剪刀、坩锅、坩锅钳、蒸发皿等
《食品检验技术》课程实验项目2
食品中蛋白质的测定
一、实验目的
掌握凯氏定氮法测定蛋白质含量的原理和方法;学会使用凯氏定氮仪。
二、实验内容
凯氏定氮法测定牛奶蛋白质的含量。
三、实验原理
消化:样品中含氮有机物与浓硫酸和催化剂一起加热消化,使蛋白质分解,分解的胺基氨与过量的硫酸结合生成硫酸胺留在溶液中,其主要反应式为:
2 NH2(CH)2COOH +13 H2SO4 = (NH4)2SO4 + 6 CO2 + 12 SO2 + 16 H2O
另外,催化剂硫酸铜在有机物全部消化后,溶液显清澈透明的蓝绿色,可用它来指示消化终点。此外,硫酸铜还可用做下一步蒸馏时碱性反应的指示剂。过氧化氢,为氧化剂,有助于有机物消化,同时可以消除消化过程中的气泡现象。
蒸馏:消化终了后所有蛋白质的氨态氮都转化成铵盐形式,硫酸铵在碱性条件下进行蒸馏,将释放出来的氨用硼酸溶液吸收,生成四硼酸氢铵.其反应式为:
(NH4)2SO4+2NaOH=Na2SO4+2NH3+2H2O NH3+4H3BO3 =(NH4)2B4O7+5H2O
滴定:用盐酸标准溶液直接滴定产生的四硼酸氢铵,根据消耗盐酸溶液的量计算样品含氮量,然后换算成蛋白质含量。
(NH4)2B4O7+2HCl+5H2O=2NH4Cl+4H3BO3。
四、实验方法与步骤
1、样品消化:准确称取牛奶1 ml,小心移入干燥的凯氏烧瓶中(勿粘附在瓶壁上)。加入0.2 g硫酸铜、0.3 g硫酸钾及10 ml浓硫酸,小心摇匀后,于瓶口置一小漏斗,瓶颈45°角倾斜置电炉上,在通风橱内加热消化。先以小火缓慢加热,待内容物完全炭化、泡沫消失后(泡沫过多时,可从小漏斗加入2-3滴无水乙醇),加大火力消化至溶液呈蓝绿色,继续加热0.5h,冷却至室温。消化过程中,若在消化管上部发现有黑色颗粒时,应小心地转动消化管,用消化液将它冲洗下来,以保证样品消化完全。同时消化1份空白试剂为对照。2份样品消化结束后均定容至10 ml。
2、蒸馏、吸收:
在水蒸汽发生器内装入蒸馏水至2/3体积处,加入硫酸1 ml,混合指示剂2~3滴,玻珠数粒,接通电源,使电炉加热,用产生的水蒸汽冲洗全套仪器,至馏出液不显酸碱性。
量取10ml硼酸溶液于锥形瓶中,加入混合指示剂2滴,置于冷凝管下端,此为接收瓶。量取1 ml样品消化液由加料口注入反应室,用5ml蒸馏水冲洗加料口,再加入400g/l NaOH溶液10 ml(溶液应呈蓝褐色)。不要摇动,立即塞紧棒状玻塞,并加少量蒸馏水,以水封加料口,以防漏气。夹紧反应室下口,用直火加热开始蒸馏,当水蒸汽吹入反应室时,准确计时,反应3 min,下降接收瓶,使硼酸液面离开冷凝管口,继续蒸馏1min,用中性蒸馏水淋洗浸入硼酸部分的管外壁,移出接收瓶,滴定。
3、滴定:将接受瓶内的硼酸液用0.01mol/l盐酸标准溶液滴定至终点。同时做一试剂空白(除不加样品,从消化开始操作完全相同)
4、结果计算:
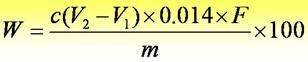 |
式中W—样品中蛋白质的含量,%;
c—盐酸标准液的浓度,mol/l;
V1—空白滴定消耗标准液的体积,ml;
V2—试剂滴定消耗标准液的体积,ml;
m—样品体积,ml;
0.014—氮的毫摩尔质量,g/mmol;
F—蛋白质系数:牛奶为6.38,一般为6.25。。
五、实验要求
实验内容要求:(1)凯氏定氮法的误差,主要因消化操作的条件而产生,因此要格外注意。(2)量取的样品倒入凯氏烧瓶时,不要将样品粘在瓶颈上,以免加入消化液后试样炭化粘在瓶颈上消化不彻底.消化过程中要逐渐升温,当低温加温至出现带有硫酸的白色气体后,才可升温使溶液沸腾,但应避免剧烈沸腾。(3)消化过程中,消化液体积不可蒸至少于原来的三分之二,更不可蒸干,若硫酸损失过多,应酌量补加硫酸。若取样量较大,如干待测样超过5克,可按每克试样5毫升的比例增加硫酸用量。
实验报告及考核评价要求:能正确、详尽书写实验目的、实验基本原理、操作步骤,正确客观的记录实验结果,并对实验结果(尤其是不理想的实验结果)进行分析和讨论。
六、场地、设备与器材
实验场地:待定
实验设备与器材:凯氏烧瓶、容量瓶、锥形瓶、酸式滴定管、消化炉、蒸馏仪、精密天平、自动搅拌器、移液枪、移液管、皮管、铁架台、铁夹、电炉、试管夹、凯氏定氮仪,回流装置,碱式滴定管、通风橱等
《食品检验技术》课程实验项目3
食品中脂肪的测定
一、实验目的
学习索氏提取法测定粗脂肪含量的原理及方法。
二、实验内容
索氏提取法测定佛手脂肪的含量。
三、实验原理
索氏(soxhlet)脂肪提取器为一回馏装置,由浸提管、小烧瓶及冷凝管三者连接而成。浸提管两侧分别有虹吸管及通气管,盛有样品的滤纸斗(包)放在浸提管内。溶剂(乙醚)盛于小烧瓶中,加热后,溶剂蒸汽经通气管至冷凝管,冷凝之溶剂滴入浸提管,浸提样品。浸提管内溶剂愈积愈多,当液面达到一定高度,溶剂及溶于溶剂中的粗脂肪即经虹吸管流入小烧瓶。流入小***溶剂由于受热而气化,气体至冷凝管又冷凝而滴入浸提管内,如此反复提取回馏,即将样品中的粗脂肪提尽并带到小烧瓶中。最后,将小烧瓶中的溶剂蒸去,烘干,小烧瓶增加之重量,即样品中粗脂肪含量。
样品用无水乙醚或石油醚等溶剂抽提后,蒸去溶剂所得的物质称为粗脂肪。所谓粗脂肪,是脂肪、游离脂肪酸、蜡、磷脂、固醇及色素等脂溶性物质的总称。因为除脂肪处还含有色素及挥发油、蜡、树脂等物,这种抽提法所得的脂肪为游离脂肪。
四、实验方法与步骤
1、将放有滤纸和白色棉线的100-105℃烘箱内,烘至恒重,记录重量为m。
2、用分析天平称取佛手干样约2g(准确至小数点后3位),用滤纸包好,并用白线捆扎好,置于表面皿中放入称量,记录重量为m1。
3、将滤纸包放入提取器的滤筒内,滤纸包高度不能超过滤筒的虹吸管,装上冷凝管和接收瓶,由冷凝管上端加入无水乙醚(约为接收瓶容积的2/3),45-50℃恒温水浴锅加热回馏2-4小时。(控制水浴温度,勿使乙醚沸腾过度,使乙醚物质循环一次时间约20min, 反复循环,直至提取筒内乙醚无色,不再有脂肪溶出为止。)
4、提取完毕,待乙醚完全流入小烧瓶时,取出滤纸包,用吹风机将残留乙醚吹尽(或直接在通风橱中挥发干后,放入表面皿内100-105℃烘箱中烘10 min,取出置干燥器中冷至室温,称重,记录重量为m2。
5、按同法,用不包样品的滤纸包做空白测定。
6、测定脂肪后,小烧瓶需先用2%氢氧化钠酒精浸泡,再用肥皂洗净烘干保存。
7、样品粗脂肪含量计算:
<, IMG src=/edit/uploadfile/20150728213142768.png width=136 height=77 >样品中粗脂肪含量 = ×100
m :表面皿、滤纸和白线的质量 g
m1:m和干样品的质量 g
m2 : m和提取脂肪后样品的质量 g。
五、实验要求
实验内容要求:(1)进行本实验时应切实注意防火,乙醚为易燃品,切忌明火加热,同时要注意提取器各连接处是否漏气,以及冷凝管冷凝效果是否良好,以免大量乙醚蒸气外逸。(2)滤纸包必须用丝线扎好,保证样品不漏散。样品包放入浸提管后,其高度不能超过乙醚面的最高高度。(3)装入乙醚之量,应以在回馏过程中小烧瓶内有适量乙醚存在为准,如发现小烧瓶中脂肪颜色变深(似烧焦状),系溶剂太少或温度太高。
实验报告及考核评价要求:能正确、详尽书写实验目的、实验基本原理、操作步骤,正确客观的记录实验结果,并对实验结果(尤其是不理想的实验结果)进行分析和讨论。
六、场地、设备与器材
实验场地:待定
实验设备与器材:索氏提取器、分析天平、恒温水浴锅、干燥器、铁架台、橡皮管、万能夹、干燥箱、电吹风、通风橱、剪刀、研钵,棉线,脱脂棉,纱布,培养皿,烧杯,试剂瓶,旋转蒸发仪,恒流泵,橡皮塞,洗耳球等
《食品检验技术》课程实验项目4
食品中Vc的测定
一、实验目的
掌握滴定法测定食品中Vc含量的原理及操作。
二、实验内容
食品中Vc含量的测定。
三、实验原理
Vc作为水溶性维生素,具有很强的还原性。还原型抗坏血酸可以还原染料2,6—二氯靛酚。该染料在酸性溶液中是粉红色(在中性或碱性溶液中呈蓝色),被还原后颜色消失;还原型抗坏血酸还原染料后,本身被氧化成脱氢抗坏血酸。在没有杂质干扰时,一定量的样品提取液还原标准染料液的量,与样品中抗坏血酸含量成正比。
四、实验方法与步骤
1、取桔子一瓣,准确称重m,置于研钵中,加入适量的1%草酸-EDTA溶液避光研磨,匀浆转入50ml容量瓶,样品中再加入少量草酸-EDTA溶液研磨,收集匀浆于50ml容量瓶,定容至50ml;过滤,备用;
2、准备滴定架:滴定液为0.001N的2,6-二氯靛酚。取10ml样品液,滴定到溶液呈微红色,并保持15秒不褪色,记录消耗的2,6-二氯靛酚溶液体积V1;
3、另取10ml 1%草酸-EDTA溶液作空白对照,记录消耗的2,6-二氯靛酚溶液体积V2;
4、计算: Vc含量(mg/100g样品)=(V1-V2)×样品提取液总体积(50ml)×0.088×100/(被检样品重量m×滴定时所取样品提取液体积) (其中:0.088代表1ml 0.001N 2,6-二氯靛酚溶液相当于0.088 mg Vc。)。
五、实验要求
实验内容要求:(1)整个实验要求避光操作。
实验报告及考核评价要求:能正确、详尽书写实验目的、实验基本原理、操作步骤,正确客观的记录实验结果,并对实验结果(尤其是不理想的实验结果)进行分析和讨论。
六、场地、设备与器材
实验场地:待定
实验设备与器材:精密天平、剪刀、自动搅拌器、滴定架、酸式滴定管、移液枪、橡皮塞,洗耳球等